流體相平衡相圖分類
流體相圖表述的是壓力、溫度、組成之間的關系,由于流體性質的差別,它們在不同條件下顯現出的相行為也截然不同,總體上可將相圖分為六大類(其中I至V類可以通過van der Waals方程定性描述,第VI類不能由其描述,此主要是具有較強氫鍵相互作用的系統),在大類下面還有小類,分類的原則主要是根據混合流體在高壓下所形成的臨界性質和相態進行的,六大類的基本壓力-溫度圖如圖(1)所示,純物質的P-T曲線終止與各自臨界點。圖中各符號意義如下:
綠色圓點——純物質臨界點;
藍色實心上三角——高溫高壓下液液共混上混溶點(UCEP);
藍色實心下三角——低溫低壓下液液共混下混溶點(LCEP);
黑色線條——流體溫度和壓力的關系圖;
紅色虛線——混合物臨界點組合;
單相區——僅單相流體存在,有且僅有一相;
VL——汽液兩相區;
VLL——汽液液三相。
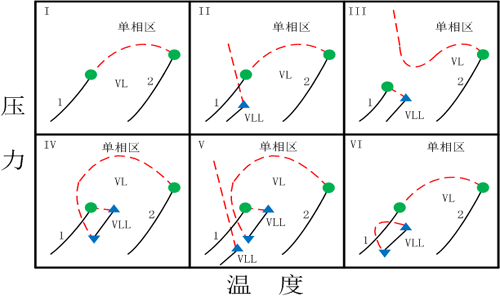
圖(1) 相圖的分類
I類相圖:該相圖在能夠涉及的溫度和壓力范圍內,不存在液液平衡(即液相完全互溶),且臨界曲線連續;在紅色臨界線上方為單相流體,下方為汽液兩相平衡區;該類混合物主要由化學性質相似、分子大小差別不大的非極性物質或弱極性物質所組成,如甲烷-丁烷、氫氣-甲烷等等體系。
II類相圖:該相圖與I類相圖相似,不同的是在較低壓力和溫度條件下存在液相互溶區,隨著壓力和溫度的升高,液相又完全互溶,如二氧化碳-碳氫體系、水-氯化氫體系等等。
III類相圖:該相圖與I類和II類不同的是,臨界線有兩個分支,一是從易揮發組份開始到上部混溶點結束,另一個是從難揮發臨界點出發,但不與易揮發組份臨界點相連接,而是產生了分裂。這種體系有水-苯、氨-氮等等。
IV類型圖:在中間溫度范圍出現液液部分互溶,易揮發組份臨界點與上部混溶點相連,難揮發組份臨界點與下臨界混溶點相連,如乙烷-醇混合物、二氧化碳-硝基苯體系等等。
V類相圖:與IV類相似,只是在低溫區有出現液液相分裂區,如甲烷-己烯、苯-聚異丁烯等等。
VI類相圖:該類型相圖是獨立于高溫汽液臨界現象之外的低溫液液平衡,而且溫度更低時有完全互溶了。產生這個現象的原因是不同組份間生成氫鍵,低溫時氫鍵加強反而促進互溶,由于這種弱化學鍵的作用,范德華方程無法給出正確的描述。
