簡單蒸餾
簡單蒸餾是指將需要處理的溶液一次性的加入或投入到某一容器中,通過加熱介質如蒸氣、加熱油等進行加入使其逐漸蒸發,蒸發出的汽相物質進入冷凝器冷卻,最終獲得需要的產品,使原溶液得到簡單的分離。在簡單蒸餾的過程中,投入容器的溶液濃度逐步發生變化,重組分濃度越來越高,而輕組分濃度越來越少;而且在蒸餾過程中,汽相組分也不斷發生變化。簡單蒸餾的基本流程如圖1所示。
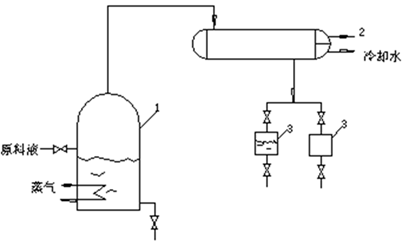
圖1. 簡單蒸餾基本流程
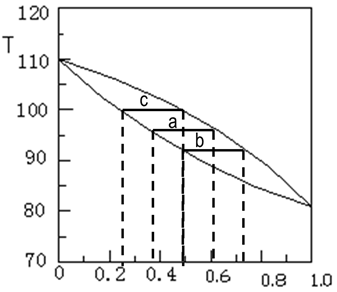
圖2 相圖表示簡單蒸餾的微分操作過程
簡單(微分)蒸餾過程的計算。假設該過程的各參量如下:
F、W ——一次性加入釜內的料液量和微分蒸餾結束后的殘液量,kmol;
x1、x2——原料液和蒸餾后殘留液中易揮發組分組成,mol/mol;
L——某一瞬間釜內的液相量,kmol;
x、y——某一瞬間的液汽組成,mol/mol。
假設經過微分時間dt后,液相量減少dL,液相組成變化了dx。以蒸餾釜為衡算范圍,則對易揮發組分,蒸餾dt前后的微分物料衡算為:
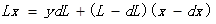
上式整理后得:

在微分蒸餾中,由于dL和dx均為較小值,因此合理假設dLdx約等于0,從而得如下方程:
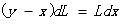
所以:
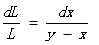
對上式進行積分,dL的變化為F變到W,與此同時dx的變化范圍為x1到x2,因此有:
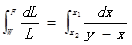
對其進行定積分計算,則得:
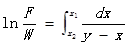
觀察上式,y為與x相平衡時的汽相中易揮發組份,必須借助相平衡性質才能獲得完整的解,也即離開相平衡性質,不可能完成蒸餾的計算。下面假設了汽液平衡的三種不同情況進行求解。
(1)對于理想溶液 ,平衡關系可表達為:
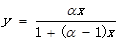
將該式代入進行積分可獲得:
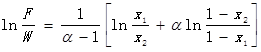
該式為簡單蒸餾的基本方程,將溶液濃度和組份及相平衡性質進行了關聯,其中α是相對揮發度。
(2)假設在簡單蒸餾的操作條件范圍內平衡線可近似地用直線表示:
y = mx + b
將該式帶入進行積分可獲得:
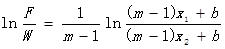
其中m是相平衡參數。
(3)假設平衡線為過原點的直線,即第(2)種情況中b=0,則積分后可得:
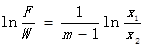
從以上計算過程可知,簡單蒸餾過程的計算實質就是物料衡算結合相平衡方程,當然這里并未涉及到冷/熱負荷的計算。
